��������p�Ɣ���p
�@
�@����̎�p�ł͂�������ׂēE�o���C����̊������߂���������p�i����זE�����S�ɓE�o�����Ɣ��f������p�j�Ƃ���ɂ���ɂ�a�炰�邱�Ƃ�g�̂̕��S���l���C����̈ꕔ��E�o����Ƒ��i�������j��p�Ƃ�����܂��B�O�҂�������p�C��҂����p�Ƃ��Ăт܂��B
�@
�@��p�Ö@�ł͂���̊��S�E�o���Ȃ킿������p�𗝑z�Ƃ��܂����C����������זE�͖ڂɂ݂��Ȃ����̂ł���C�]�ڂɂ��E�o�ł��Ȃ��������ʂ��炪�Ĕ����邱�Ƃ͑����C�����S����肫�ꂽ�Ɣ��f�ł���͎̂��͂̏����̃����p�߂ɓ]�ڂ��Ă���i�K�܂łŁC����ȏ�i�s���Ă���ƍ�����p�͓���Ȃ�܂��B
�@���������Ď�p�͓]�ڂ��N�����O�̏����̒i�K�ɂ����ėL���ƍl���Ȃ���Ȃ�܂���B���݂͐i�s����Ȃǂɂ͎�p�̑��ɕ��ː��Ö@��R����܂p����W�w�I���Â��嗬�ƂȂ��Ă��܂��B
�@ |
|
���g���p�Ək����p
�@
�@�Ĕ��̖h�~��ړI�Ƃ��C���L���͈͂����p���g���p�C�̂̃_���[�W�╉�S���y�����邽�ߐ؏�����͈͂��ŏ����ɂƂǂ߂��p���k����p�Ƃ����C����̎�p�Ö@�͌��݂��̓�̕����Ői��ł��܂��B
�@
�@�k����p���i�߂������Ŋg���p���i�߂��Ă���̂́C��������悤�ł�����܂����C�����Z�p��p��̊Ǘ��Z�p�C��t�̐i���Ȃǂɂ��C�]���͂���̑��݂��F�߂��Ă��؏���������߂���Ȃ��������ʂ̎�p���\�ɂȂ������߂ł��B
�@�܂����ꂼ��̑���̏��������p�߂ւ͓]�ڂ��₷�����߁C�a���������łȂ��C�\�h�I�Ƀ����p�߂܂Ŏ�菜���C�����p�ߊf���i���������j�������Ȃ��邱�Ƃ������Ȃ�C�Ĕ��h�~�Ƃ����_�Ő��ʂ������Ă���Ƃ����Ă��܂��B |
|
|
���g���p
�@�g���p�͐��ʂ������Ă���Ƃ�������������܂����C����ł͔ے�I�ȍl��������܂��B�Ȃ��Ȃ�C�l�Ԃ̂��炾�͑����̊튯���A�g�������ċ@�\���Ă�����̂ł���C�g�債�Đ؏�����قǁC�g�[�^���Ƃ��Đ������ێ�����\�͂�p�n�k���ቺ���Ă��܂�����ł��B
���݂���̕W����p�c�Q�s���Ɗg���p
�@�i�s�݂���̎��ÂŁC�݂̎��͂̃����p�߂��L������g���p�ƁC ���͈͂̐؏��ɂƂǂ߂�W���I�Ȏ�p�i�c�Q�s���j�ł́C���Ì��ʂɂقƂ�Ǎ����Ȃ��Ƃ����������ʂ���{�̍�������Z���^�[���܂Ƃߔ��\���܂����B
�@
�@�������Z���^�[�����a�@�̍��q�O�×����@���́u�����p�߂𑽂��Ƃ������ƂŁC���҂̏�Ԃ����������Ă���\��������C�W������ �͂c�Q�s���ƍl����ׂ��ł���B�v�Ƙb���܂����B
�@�������C �P�X�X�X�N�I�����_�ōs��ꂽ�݂����p�̑�K�͂Ȕ�r�����̌��ʂ́C���{�̕W���I�Ȏ�p�c�Q�ɂł����C�^��𓊂���������̂ł����B
�@
�@���݂̈���̔�r�����̌��ʂł́C���{�ł̕W���I���ÂƂ���Ă����݂̎��͂̃����p�߂̑�Q�Q�ƌĂ��͈͂܂Ŏ�菜���c�Q��p�́C��苷���͈͂̃����p�߂���菜���c�P��p���C�T�N�������ł͂قړ������������̂́C��p���̎��S���⍇���ǂ̔������ŏ����Ă��܂����̂ł��B
���X������̕W����p�Ɗg���p
�@�X������i�X�����Z�����X�NJ��j���Â̌����ł̓����p�ߊf���݂̂̕W����p�ƃ����p�߁E�_�o�p�̍L�͈͊f�����s���g���p�Ƃ��r�����ꍇ�C�R�N���������W����p�łQ�X�D�R���C�g���p�łP�T�D�P���Ɖ�����C���̃P�[�X�ł̊g���p�͐������̒ቺ�������C�������ʂ̂Ȃ����Ƃ𗧏��Ă��܂��B
���g���p�̖��_�@
�@�����p�߂͂���זE��}���铭���̂��郊���p�����W�܂镔�ʂł�����C�g���p�ɂ�郊���p�ߊf���ɂ��Ɖu�͒ቺ�����_�Ƃ��ĂƂ炦�Ȃ���Ȃ�܂���B���̊f���͂���ɐ_�o�@�ۂ����ؒf���C�@�\��Q���N�������Ƃ�����܂��B
�@��t�̊Ԃł��C�Ĕ��Ƃp�n�k�̃o�����X���l����ƁC�ǂ��܂Ő؏����ׂ����ӌ����������Ƃ���ł��B������ɂ���g���p�͑̂ւ̃_���[�W��Ɖu�͂̒ቺ�C�p��̂p�n�k�̒ቺ���傫���Ȃ邱�Ƃ��o�債�Ȃ���Ȃ�܂���B
�@
�@�܂��C���Â̎�p�Ɍ��炸�C�����Ԃɂ킽��悤�ȑ傫�Ȏ�p�͍זE�̐��̔����ɂ��C�S�g���̉��ǔ������N����C���ꂪ������s�S�Ȃǂ̍����ǂɂȂ���v�����ɂȂ邱�Ƃ�����܂��B
|
|
���k����p
�@�Ĕ����l������ƈ��Ղɐ؏��͈͂��k�����邱�Ƃ��댯������܂����C�k����p�͑̂ւ̕��S�����Ȃ��C��p��̊��S�ȎЉ�A���\�ł���C�����̃����b�g������܂��B
�@���̏k����p���i��ōs����悤�ɂȂ������R�Ƃ��āC�ߋ��̃f�[�^���瑁������̏ꍇ�C�؏�����K�v�����Ȃ����ʂ��킩��悤�ɂȂ������ƁC�f�f���u��f�f�@�̐i���ɂ�葁���̂���̔������\�ɂȂ������ƁC���ː��≻�w�Ö@�̐i���Ŏ��Â�₤���Ƃ��ł���悤�ɂȂ������ƂȂǂ��������܂��B
�@
�@�ߔN�͈�Ê��⎡�ËZ�p�̐i���Ȃǂɂ��C����̓�����@�\���ł��邾���c���悤�ɂ���@�\������p���i��Ŏ��������悤�ɂȂ�܂����B
�@�A���̔����@�\��r�@�\�C���@�\�Ȃǂ��n�ߑ����̕��ʂŋ@�\����������H�v������C�T�d�ɍs����悤�ɂȂ��Ă��܂��B����ɂ͊��҂̎�p��̂p�n�k���d������Ƃ����l�������L�܂��Ă����w�i������܂��B�܂��J�������Ɏ�p���\�ȓ�������p�╠�o����p���}���ɕ��y���Ă��܂��B
����������p�@
�@���������ẤC�J�������ɍs�����Ƃ��ł��C���Â̂Ȃ��ł�����߂ĐN�P�����Ȃ��C���҂ւ̕��S���y�����Âł��B����҂ł��\�ŁC�Ö��������s�����Ƃŋ�ɂ����Ȃ���p�ł��B
�@�J����p�Ɣ�r���āC���@���Ԃ������ȉ��Ə��Ȃ��C�����ɎЉ�A���\�ŁC�p�n�k�̒ቺ���قƂ�ǂȂ��C���Ô�J����p�ɔ�r���Ĉ����Ƃ����Ƃ������b�g�ƌ����܂��B
�@�������C��������܂��B����߂ď��Ȃ��p�x�ł͂���܂����C�o������E�i�����j�Ȃǂ̎��̂��N���邱�Ƃ�����Ƃ������Ƃł��B
�@�܂��C���������Â͊J�����Ȃ����߁C���Âł��镔�ʂ͌����܂��B���É\�ȕ��ʂ́C�H���C�݁C�咰�C�Ȃǂ̏����ǂ⋹�o�C�_�X�C�N���Ȃǂł��B�܂������p�ߓ]�ڂ��Ȃ��C��ᇂ����ׂĈꊇ�؏��ł��鑁���̑傫���ł���C���g�D�^�������^�Ȃǂ̏���������܂��B
�@�����ǂ̂���ł́C�������̐�[���烊���O��̐j���i�X�l�A�j���o���āC�����ɂ͂߁C���̃X�l�A���i�荞�ނ��Ƃɂ���ĕa����ˏo�����C�����g�d���𗬂��ďĂ���Ƃ����|���y�N�g�~�[�ƌĂ�鎡�Ö@��a���̔S���̉��ɐ����H�����𒍓����Ă���a�����オ�点�C�X�l�A�ł܂݂����C�Ă���Ƃ����S���؏��p�i�d�l�q�j���s���Ă��܂��B
�@�܂��C�ߔN�ł͔S�����w�����i�͂���j�p�i�d�r�c�j���m������CIT�i�C�t�̊J���ŕa�ς̑傫���ɂ�����炸�C�����̏ꍇ�����̂���ł���Έꊇ�؏����\�ƂȂ�܂����B
�����o������p
�@���o���ƌĂ��J���������C�J�������C�J�����⎡�Ê������C���������o���ŏ����̐؊J�Ŏ�p���s�����@�o������p�ƌ����܂��B�@
�@�@
�@���̎�p�́C�J����p���Q�O�����ȏ�ɑ傫���؊J���Ȃ���Ȃ�Ȃ��̂ɑ��āC�؊J�������T�����ȉ��Ə��������߁C���҂̕��S�����Ȃ��C�p��̒ɂ݂����Ȃ��C�P�`�Q�T�Ԃőމ@�ł���Ƃ��������b�g������܂��B
�@���̎�p���������ꂽ�̂͂P�X�X�O�N�㏉���ŁC�����̓����p�߂̊s�����ł��Ȃ�������C�E�o���镔�ʂ����肳��Ă��܂������C���̌�Z�p�̐i���ɂ��C�K���͈͂��g�債�Ă��܂��B
�@���o����p�͍��x�ȋZ�p���v������C�{�݂ɂ���Ă��i��������̂ŁC���Ð��Ȃǂ悭�������Ă����������̂ł��B�܂��W���I�Ȃ��ÂƂ���Ă͂��܂��C���������ɕ��y�����W���鎡�Ö@�ł���ƍl�����܂��B
�@ |
|
|
���Z�J���h�I�s�j�I����������C�p�n�k�̊m�F�� �@
�@��p�ɂ����Ă͍Ĕ��̖h�~��D�悳���邩�C�p��̃_���[�W���ŏ����ɗ}���邱�Ƃ�D�悷�邩�ŁC�ǂ��܂Ő؏����ׂ������f������Ƃ��낪����܂��B
�@�����p�߂̊f���Ȃǂ́C��t��a�@�̍l���ɂ��C���傫���s���Ƃ���Ƃ����łȂ��Ƃ���ƍ�������C���̎�p���{���ɕK�v�Ȃ̂��C���ɑI�����͂Ȃ��̂��C�Z�J���h�I�s�j�I����������C��p�͐T�d�ɍs���������̂ł��B�@
�@������ړI�Ƃ�����p���������Ď����𑁂߂Ă��܂����Ƃ�����܂��B�܂���p��ɂǂꂾ���p�n�k���ۂĂ�̂��C���Ȃ킿�ǂ̂悤�ȕs���������̂���t�ɂ悭�m�F���܂��傤�B
|
�@

|
|
| ���ː��Ö@ |
 |
�����ː��Ö@�Ƃ�
�@X����K���}���Ȃǂ̓d���g������זE�֏Ǝ˂��邱�Ƃɂ���āC����זE�����ł�������@�ł��B��p�Ɣ�r����C�傫�ȕό`���������ɍς݁C���̓I���S�����Ȃ��Ƃ������Ƃ������b�g�ł��B���ː��Ö@�͎�p�Ɠ����悤�ɋǏ��Ö@�̈�ł���C��p�≻�w�Ö@�ƕ��p���āC�傫�Ȍ��ʂ������邱�Ƃ��ł��܂��B
�@
�@���ː��ɂ����ʂ̂��邪��͂�����x���肳��܂��B���Ƃ��Δ����a�C�_�o��זE��C���������p��C�G����炪��C�B����C�N������C�]��ᇁC������C�����m�[�}�Ȃǂ͌��ʂ�����Ƃ���Ă��܂����C�咰����C�̑�����C�O���B����Ȃǂ͊����Ⴍ�C����܂ł̎��Õ��@�ł͌��ʂ����܂���҂ł��Ȃ��ƌ����Ă��܂��B�@
�@���ː��͎��͂̍זE�����ł�����̂ŁC����זE�̔픚�������ł����Ȃ����邽�߂ɁC��p���Ɋ����ɏƎ˂���p���Ǝ˖@�C�����ȕ��ː�������a���ɖ��ߍ��݁C�K���}���ɂ�鎡�Â��s�����������Ö@�Ȃǂ�����܂��B
|
�@�@
|
���V�������ː��Ö@
�@���ː����Â̗��z�́u����זE�ɂ͍ő�̐��ʂ��C����זE�ɂ͍ŏ����̐��ʂ��v�Ƃ������t�ŕ\�������悤�ɁC����זE�݂̂Ƀs���|�C���g�ŏƎ˂��邱�Ƃł��B
�@
�@�������C����זE�͑̂̓����ɂ��邽�߁C���ː�������זE��˂������Ȃ��ƁC����זE�ɂ͓��B���܂���B���������āC�����̊p�x���炪��זE�֏W�����ďƎ˂��邱�ƂŁC����זE�ւ̉e�����ɗ͌��炷�Ƃ������@�����݂��Ă��܂��B���̕��@�͒�ʕ��ː����Â܂��̓��W�I�T�[�W�F���ƌĂ�Ă��܂��B�܂����q�����g�������Âł́C����זE�����ōő�̃G�l���M�[��������悤�R���g���[������Ă��܂��B
�����q������
�@�ߔN�C�T�C�N���g�����i�~�`������j��V���N���g�����i����������j�Ȃǂ̉�������g���āC�z�q��Y�f�̌��q�j���������C����ɏW�����ďƎ˂��鎡�Ö@���m������܂����B�@���q�̂Ȃ��ł��z�q���g�����q�����Â�z�q�����Âƌ����C�Y�f�̌��q�j���g�����Â��d���q�����Âƌ����܂��B
�@���̗��q�����Â̓����͗��q���^�����~���钼�O�ɍő�̃G�l���M�[����o����Ƃ��������i�u���b�O�s�[�N�j�𗘗p���C����a�������ŗ��q���ő�̃G�l���M�[����o����悤�R���g���[������Ă���Ƃ������ƂŁC�]���̕��ː����Âł͍���ł������X���Ȃǂ̂��Âɂ����ʂ������Ă��܂��B
�@���ɏd���q�����Âł́C�w����K���}���ŎE���Ȃ��^�C�v�̂���זE���E�����Ƃ��ł��܂��B�������݂⒰�̂悤�ɕs�K���ɓ��������C�����a�̂悤�ɑS�g�ɍL�����Ă��邪��C�L���]�ڂ�������ɂ͓K���ł����C���ʂ͌Ō`��ᇂɌ��肳��܂��B
���K���}�i�C�t
�@���̎��Ñ��u�́C�w�����b�g�^�̌Œ������҂̓����ɂ��Ԃ��C���̃w�����b�g�^�̌Œ���C�R�o���g�U�O�Ƃ������ː����C����זE�̂P�_�ɏW�����ĕ��˂����Ƃ������̂ŁC�]��ᇂ̎��ÂɎg�p����C�i�C�t�Ő������悤�ȃV���[�v�Ȍ��ʂ������邱�Ƃ���C���̂悤�ɌĂ�Ă��܂��B�R�O�N�قǑO����n�܂�C�]��ᇂɂ͎��Î��т�����܂��B�������C���҂̓����͓����Ȃ��悤�����ł�������ƌŒ肳���K�v������܂��B
���T�C�o�[�i�C�t
�@�K���}�i�C�t������ɐi�����������Ê킪�T�C�o�[�i�C�t�ƌĂ����̂ł��B���̎��Ö@�ł͎��R�Ȉʒu�Ɗp�x����ア�w���������̂P�_�ɃR���s���[�^����̃��{�b�g�ɂ��W�����ďƎ˂��܂��B�Q��̂w�������p�J���������҂̓��������j�^�[���C���҂̃Z�b�g�A�b�v���̂���⎡�Ò��̔����ȓ����������I�Ɍ��o���C�r�[�������܂��B�@
�@���̑��u�ł͕a���ʒu�̊m�F�̂��߁C���b�V����̃}�X�N�����܂����C�K���}�i�C�t�ƈقȂ�C�����������ŌŒ肷��K�v������܂���B
�@���{�ł͂܂����̔]��ᇂ⎨�@�ȁC���o�O�Ȃ̎�ᇂȂǂɌ��肳��܂����C���̕����ŃA�����J�Ȃǂł͔x������X������ւ̎��Â��s���C����זE�ւ̃_���[�W�����Ȃ����Ƃ��獡��̔��W�����҂���܂��B
���w�i�C�t�E�A�L���i�C�t�i���j�A�b�N�i�C�t�j
�@�]������g�p����Ă������j�A�b�N�܂��̓��C�i�b�N�ƌĂ�钼���������ː����Ê�ɂw�i�C�t�ƌĂ��V�X�e����g�ݍ��ނ��ƂŁC�a�����ɑ��������琳�m�ɂP�����`�Q�����Ƃ����덷�ŏW���Ǝ˂��\�ƂȂ�܂����B�܂��A�L���i�C�t��g�ݍ��ނ��Ƃŕa���̌`�ɍ��킹���s���`�Ǝ˂��\�ƂȂ�܂����B
�@
�@�K���}�i�C�t�ƈ���đ�����Ǝˁi�����Ǝˁj���ł���̂ŁC�a�ϕ��ʎ��ӂ̐���זE�ւ̉e����Ⴍ�}���邱�Ƃ��ł��܂��B�܂��K���}�i�C�t���傫�ȕa�������Âł��܂��B���Ð��т̓K���}�i�C�t�Ɠ����x�Ƃ����C��ɓ�����Ɏg�p����C�O���B����ȂǑ̊����̂���ɂ��Ǝ˂���������Ă��܂��B�S���̊�a�@�ō̗p����Ă��܂��B
���g���Z���s�[
�@��������ː����Ñ��u�g���Z���s�[�iTomoTherapy�j�����E�I�ɒ��ڂ���Ă��鎡�Ê�ł��B���̃��J�j�Y���͕��ː��Ǝˑ��u�Ƀw���J���b�s�̌��������p���C���ː��r�[�����点���ɉ�]�����Ȃ��犳���̂ݐ��m�ɏƎ˂��邱�Ƃ��\�ɂ������̂ł��B���̑��u�̓s���|�C���g�Ǝ˂��\�Ȃ����łȂ��C���G�ȕa����C��x�ɕ����̎�ᇂɑΉ��ł���Ƃ��������b�g������܂��B
�@�]���͓���Ƃ���Ă����O���B����⑽�����x����Ȃǂ̕��ː����Â��\�ƂȂ�C�W���Ǝ˂���L�͈͂ȏƎ˂܂ʼn\�Ȃ��߁C�T�C�o�[�i�C�t��w�i�C�t��葽���̂���ɑΉ��ł��܂��B
���m�o���X
�@�m�o���X�ƌĂ�鋭�x�ϒ����ː����Ê���o�ꂵ�Ă��܂��B��������낢��ȕ������痧�̏Ǝ˂��ł��܂����C�Ǝ˂���ʂ̕a���̌`��ɍ��킹�ăr�[���̌`�C���x���u���ɕω������邱�Ƃ��ł���Ƃ�������I�Ȃ��̂ł��B����ɓ��̒ǐՑ��u���g�ݍ��܂�Ă���C����a���ւ̐��m�ȏƎ˂��\�ł��B
�@�Ǝˈʒu���肪�����ŏ�������C�����ɍ��G�l���M�[���W���ł��邽�߁C���Î��Ԃ��Q�O���`�R�O���ƒZ���C�O���ł����Â��\�Ƃ��������b�g������܂��B���j�A�b�N��p�����w�i�C�t����ɓ���ᇑΏۂł���̂ɑ��C����ȊO�ɂ��̑�����C�x����C�Ғł���C�O���B���S�g�̂��Â��\�ł��B
�@���ʂ͎�p�Ɠ���������ȏ�ƌ����Ă��܂����C�s���|�C���g�Ǝ˂ӂƂ��Ă��邾���ɁC�L�͂ȉ��u�]�ڂ��ᇂ̌`���͂����肵�Ȃ��^�̂��̂ɂ͎g���܂���B
���t�H�[�J�����j�b�g�@
�@���ː����Ñ��u�i���C�i�b�N�j�Ƃb�s����̉����������u�ł��B���ː����Â̑O�ɂb�s�ŏƎ˂��镔�ʂ��m�F���C�Ǝ˂��邽�߁C�����x�̎��Â��\�ł��B���ː��̈ʒu���c�E���E�����̎O�����ŕω���������̂ŎO�����t�H�[�J�����j�b�g�Ƃ��Ă�Ă��܂��B
�@
�@���̑��u�͓��{�ŊJ�����ꂽ���̂ŁC���̋@���v�����A���@�����ɂ��ƁC���ʕ������Ȃ킿���ŕω�������Ǝ˂�������זE�ւ̉e�������Ȃ��C�����ʂ��傫���Ƃ������Ƃł��B�i���}�Q�Ɓ|�u���邢���Áv�����p�j
�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�A�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�@�B
 |
 |
 |
�@�}�@���Ǝ�
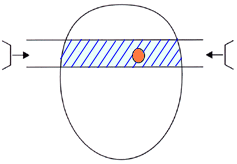
�@
�@����i�}�̊ۈ�j��W�I�Ƃ��Ė��̕�������Ǝ˂���Ɛ���זE�i�}�̃A�~�����j�ɂ������ʂ̕��ː���������B����זE�Ƀ_���[�W�i����p�j���ł�̂ŏ��ʂ����������Ȃ����L���͈͂ɂ�����ɂ͌������@�B |
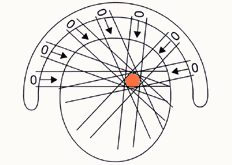
�@�}�A���s���|�C���g�Ǝˁ@
�@
�@����i�}�̊ۈ�j��W�I�Ƃ��ĕ����̕�������Ǝ˂���B
�@�ꌩ�������ǂ������Ɍ����邪�C�߂��̐���זE�̃_���[�W�i����p�j�͐}�@�ƂقƂ�Ǖς��Ȃ��B |
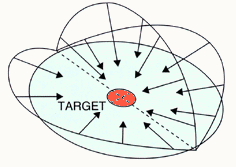
�@�}�B�O�����s���|�C���g�Ǝ�
�@
�@���낢��ȕ��ʂ̂��낢��ȕ�������Ǝ˂���B1�J���ɂ�������ː��͏��ʂȂ̂Ő���זE�Ƀ_���[�W���o�����ɕW�I�̎�ᇂɂ͑�ʂɏW����������B�_���[�W�����Ȃ����Ƃ́C���ւ̓��Ǝ˂ł͓����������邪�C�O�����s���|�C���g�Ǝ˂݂̂ł͂߂����ɔ����Ȃ����Ƃ����������B |
�@
 |
�@���̃t�H�[�J�����j�b�g�ł͂T�������x�̓������؏������ɁC���Âɐ������Ă���C���̑��傫�Ȕ]��ᇁC�x����C�̑�����C���������p��̎��Âɂ��D���т������Ă���Ƃ̂��Ƃł��B�@�@
�@�܂��A�����̓t�H�[�J�����j�b�g�����ǂ��C�x����Ȃnjċz�ƂƂ��ɓ�����ᇂ�ǐՏƎ˂��郁�J�j�Y���i�`�F�C�V���O�r�[���j��������C�X�[�p�[�t�H�[�J�����j�b�g�Ƃ��Ċ��������Ă��܂��B
�@���̃t�H�[�J�����j�b�g��s���|�C���g�Ǝ˂��ڂ����m�肽�����́C�A�����̒����u���邢���Áv���Q�l�ɂ��Ă��������B |
|
|
|
|
|
|
|
|
|
|
|
|
���ŐV���ː����Ê�̃����b�g�@
�@���ː����Â̓����p�������炵�C�畆���Ԃ��Ȃ�����C�������N�����Ȃǂ̕���p������܂��B�܂��x�����̕���p�͒����ɂ킽�邱�Ƃ�����܂��B�����̍ŐV���ː����Ê�͊����̂݃s���|�C���g�ŏƎ˂ł��邽�߁C����זE�Ƀ_���[�W��^�����C�����̕���p���ŏ����ɗ}���C����זE�������I�Ɏ��ł����邱�Ƃ��ł��܂��B
�@���{�͉��ĂƔ�r���āC���ː����Â̕���ł͒x����Ƃ��Ă���ƌ����Ă��܂��B����͐i�s�x�������x�̂���ł����Ă����ː��Ŏ��Â��Ă���̂ɑ��C���{�ł͎�p�Ő؏����Ă���P�[�X�������Ƃ������R�ɂ����܂��B
�@
�@���ː��ɗL���Ȃ���͑O�q�����悤�ɂ�����x�����܂����C���̂悤�ȍŐV�@����g�������Âł͑傫�Ȑ��ʂ�����Ă���C���p���������̂ł��B���������ɐݒu�������Ȃ����Ƃ���_�ł����C�ŐV���ː����Ë@��ݒu�a�@�̃y�[�W�ŏЉ�Ă��܂��̂ŎQ�l�ɂ��Ă��������B

|
|
| �R������� |
 |
���R����܂Ƃ�
�@
�@�R����܂͂��ꎩ�̂�������E���\�͂����������̂ł���C���^���@�Ƃ��Ă͐Ö����˂�o�����^�Ȃǂ�����܂��B�܂������֒��ړ��^������@������܂��B
�@
�@�R����܂͂����邪�ÂɎg�p����܂����C���ː��Ö@���p�Ö@�̕⏕�Ö@�Ƃ��āC�p�O��p��ɓ]�ڂ��Ă��邪����k��������ړI�Ŏg�p�����ꍇ��C�����a��S�g�ɍL�������i�s�����}������Ƃ����ړI�Ŏg�p�����ꍇ������܂��B
|
�R����܂̎�� |
���R����܂̎��
�@�R����܂͂���זE�ɑ����p�̈Ⴂ�Ȃǂɂ�肢�����ɕ��ނł��܂��B
| ����ӝh�R���@���\�g���L�Z�[�g�C�V�^���r���C�t���I���E���V���C�����J�v�g�v�����C�Q���V�^���r���Ȃ� |
�@���B�̐���Ȃ���זE�ɑ����܂܂��y�f�𗘗p���āC�����}���������Ƃ����ł��B��ӝh�R�܂̓v���h���b�O�Ƃ����āC�{���̓���������O�̉��w�\������������Ƃ��ē��^����܂��B
�@���ꂪ����זE�̒��ɂ���y�f�̓������Ċ���������C����זE�����Ɏ��炵�߂܂��B�������C���̍y�f�͐���זE�ɂ����݂��邽�߁C����זE���_���[�W���邱�ƂɂȂ�܂��B |
|
| ���A���L�������@�V�N���t�H�X�A�~�h�C�C�t�H�X�t�@�~�h�C�_�J���o�W���C�`�I�e�o�C�j���X�`���Ȃ� |
�@�}�X�^�[�h�K�X�Ƃ����ŃK�X����̌����̌��ʊJ�����ꂽ��ł��B�A���L�����܂͂c�m�`�ƌ������C�c�m�`�������C�זE���ɂc�m�`��j�C����זE�����Ɏ��炵�߂܂��B�@
�@����͍זE�łƌĂ��Ŗ�ł��B���������Đ���זE�ɂ��_���[�W��^���邾���łȂ��C�c�m�`�����͐���זE�̂��𑣂��\��������܂��B |
|
| ���R���R�������@�_�E�m���r�V���C�C�_���r�V���C�h�L�\���r�V���C�u���I�}�C�V���C�s�����r�V���Ȃ��@ |
| �@�������������ꂽ���̂ŁC��ʓI�ȍR���������ۂ����ł�����̂Ɠ��l�ɁC����זE�����ł�����R�������ł��B��������Ȍ����͂���זE�̂c�m�`�����j�Q�ƁC�c�m�`���̐ؒf�ł���C���������Đ���זE�ɂ��e����^���C����p�Ƃ��Ĕ����a�C�S�؏�Q��x�@�ۏǂ��N�������Ƃ�����܂��B |
|
| ���A���A���J���C�h�@�C���m�e�J���C�r�m�����r���C�r���N���X�`���C�G�g�|�V�h�C�h�Z�^�L�Z���Ȃ� |
| �@�A��������ꂽ��܂ŁC�זE���ɋ@�\��������ǂƂ������̂̓�����j�Q���C����זE�����ł����܂��B�����������ǂ͐_�o�זE�ł��d�v�ȓ��������邽�߁C�葫�̂��т�Ȃǂ̐_�o��Q���N���邱�Ƃ�����܂��B |
|
| ���v���`�i�����@�V�X�v���`���C�l�_�v���`���C�J���{�v���`���C�I�L�T���v���`�� |
�@�v���`�i�̓d�ɂ��g���čۂ̔|�{�������Ȃ��Ă���Ƃ��ɁC�d�ɂɎg���Ă���v���`�i���|�{�t�ɗn���C�E�ۍ�p�����������ɕω����Ă��邱�Ƃ��킩��C�R����܂Ƃ��Ă��g����悤�ɂȂ�܂����B
�@�������܂͂���זE�̂c�m�`�ƌ������邱�ƂŁC�c�m�`�̕�����W���C����ł��Ȃ��Ȃ�������זE�����ł����܂��B�@�ق��̍R����܂ł͌����Ȃ��ꍇ���ܑϐ�������������זE�ɑ��Č��ʂ�����̂������ł��B�@ |
|
�����q�W�I�����@���c�L�T���C�Q�t�B�`�j�u�i�C���b�T�j�C�n�[�Z�v�`���C
�@�@�@�@�@�@�@�@�@�@�@�@�@ �C�}�`�j�u�i�O���x�b�N�j�C�G�����`�j�u(�^���Z�o�j
|
�@�]������g�p����Ă���R����܂́C����זE�Ɛ���זE�̍\������ʂł����ɁC����זE����p���Ȃǂ̖Ɖu�זE�܂Ń_���[�W��^���Ă��܂��Ƃ�������p������܂����B����������݂̂������ٍ\�����𖾂���C���̓��ٍ\���݂̂ɓ������q�W�I���ÖJ������Ă��܂��B
|
|
|
���R����܂̖��_
�@�R����܂̖��_�́C����זE�ɂ��_���[�W��^���C�q�f�C�����C�E�тȂǑ����̕���p�����ƂƁC�Ɖu�זE�̗͂܂Œቺ�����Ă��܂����Ƃ��������܂��B
�@�܂��R����ܓ��^���Đ����c��������זE�́C���̖�܂ɑ��Ē�R�͂�������ւƕω����Ă��܂����Ƃ������C���������ĈقȂ�����ނ̍R����܂��ɕ��p���鑽�ܕ��p�Ö@���K�v�ł��B
�@�@�@ |
|
���V�����R�������
�����q�W�I�����@
�@�ߔN�̕��q�����w�̐i���ɂ��C�����������ٍR���₪��̑��B�������N�����y�f��^���p�N�����炩�ɂȂ�C�����ɏW�����Ă͂��炭��܂��J������C���q�W�I��ƌĂ�C�傫�Ȍ��ʂ��������Ă��܂��B
�@
�@���̖�܂͂���܂ł̍R����܂ƈقȂ萳��זE�ւ̉e���͂Ȃ��Ƃ���Ă��܂������C�ꕔ�ɗ\�z�O�̏d�Ăȕ���p������Ă��܂��B
�����c�L�T��
�@���������p��̎��ÂɎg���C�����p��̂b�c�Q�O�R���ɂ͂��炭���m�N���[�i���R�̂ŁC�P�ƂłR�O���ȏ�̑t�����������Ă��܂��B
���Q�t�B�`�j�u�i�C���b�T�j
�@���זE�x����̎��ÂɎg���C����̑��B�ɊW����`���V���L�i�[�[�Ƃ����y�f��j�Q�����܂ł��B�Q�O���̊��҂̎�ᇂ��k����,��ᇂ̐����̒�~�܂Ŋ܂߂�ƂU�O���̊��҂Ɍ��ʂ��������Ƃ���������܂����C�ꕔ�ɋ}���x��Q��Ԏ����x���Ȃǂ̕���p������Ă��܂��B
�@���̕���p�͓��ɕ��ː����Â������҂ɑ����Ƃ����f�[�^������܂��B���ː��ŏ������זE���C������鎞�ɔ������郌�Z�v�^�[���זE�̑��B�Ɋւ�����̂ŁC����͂���זE���������Ă��郌�Z�v�^�[�Ɠ������̂ł��B���������đ��B���悤�Ƃ��鐳��זE�܂ł����̎��Ö�̉e�����Ă��܂����Ƃ�����p�̌����ł���ƍl�����Ă��܂��B
���n�[�Z�v�`��
�@�����ÂɎg���C�@����זE�̕\�ʂɑ��݂���g�d�q�Q��e�̂Ɍ��т��R�̂ŁC�]�ڐ��̓�����̒��ł��C�g�d�q�Q���z���Ɣ��肳�ꂽ���҂݂̂Ɍ��ʂ�������Ă��܂��B�@���w�Ö@�Ƃ̕��p�őt����������Ԃ̉����������C������̐V�������Ö�Ƃ��Ċ��҂���Ă��܂����C�ꕔ�S����Q�Ȃǂ̕���p������Ă��܂��B
���C�}�`�j�u�i�O���x�b�N�j
�@���������������a�iCML�j������NJԎ�����iGIST�j�̎��Ö�ł��B�ُ�זE���Y��������a�b�q�|�`�a�k�`���V���L�i�[�[�Ƃ����y�f��I��I�ɑj�Q����͂��炫������܂��B���݁C�����̎��a�ɑ��č����Տ��I�L�p�����F�߂�C���ڂ���Ă����܂ł��B�������C�f���C�C���������ǂ��͂��߂Ƃ��镛��p���ꕔ�̊��҂ɔF�߂��Ă��܂�
���G�����`�j�u(�^���Z�o�j
�@�זE�x����̎��Ö�ŃC���b�T���l����̑��B�Ɋւ��`���V���L�i�[�[��W�I�Ƃ��C���̂͂��炫��j�Q���܂��B���w�Ö@�������҂≻�w�Ö@��̂������҂�Ώۂɂ����Տ������ł́C�U�^�Q�̉��������ςS�E�V�J���������̂ɑ��^���Z�o���^�Q�͕��ςU�E�V�����������C�L�Ӎ����������Ƃ��āC�������J���Ȃɏ��F���̐\�������Ă���Ƃ���ł��B
�����q�W�I���Ö�̖��_
�@����זE�ɉe����^���Ȃ��C����I�Ȃ���̎��Ö�Ƃ��ĊJ������C���҂��ꂽ���q�W�I���Ö�ł����C���ʂ�����̂͊��҂̈ꕔ�ł���C�܂��C���i�s���Ă����ƌ��ʂ�����Ă������Ƃ������Ƃ������Ƃ��킩���Ă��Ă��܂��B
�@����͂���̕ψق�����`�q�͂P��ނł͂Ȃ���������C�i�s����ƈ�`�q�̕ψق��������C�Ή�������Ȃ����Ƃ����ʂ�������Ȃ������̈�ƍl�����Ă��܂��B
�@�܂��C�ꕔ�̊��҂ɂ͏�L�Ɏ������悤�ȕ���p�������C�{���Ȃ�e�����Ȃ��͂��̐���זE�ɂ��e����^���Ă���P�[�X���l�����܂��B
���V�����R����܂̗��p���@�@
�@�ߔN�C�R������Â̌���ł́C���k�����Ȃ��Ă��C�����ɂ킽�葝�B���Ȃ��Ȃ炻������ʂ�����Ƃ���l�������L�܂����܂��B
�@����͑�ʂ̍R����܂ɂ�肪��̎�ᇂ��k�����Ă��C�Ɖu�זE�����߂Ƃ��鐳��זE���_���[�W���Ă��܂��C���ʂƂ��ĉ����ɂȂ���Ȃ����Ƃ������Ƃ������Ƃ�C���k�����Ȃ��Ƃ�������x�̑傫���ő��B���Ȃ��Ȃ����Ƃ̋����Ƃ����`�ʼn����ł��邱�Ƃ��킩���Ă�������ł��B
�@���̂悤�ȍl��������C�R����܂̓��^��ʏ��菭�Ȃ��ʂ���n�߁C����p�����������C����������p���[���ł͂Ȃ��Ƃ����ʂɎ���܂œ��^�ʂ��������Ȃ���C�����Ԃɂ킽�肪�Â𑱂���Ƃ������@���s���Ă���Ƃ��������C�u����x���Ö@�v�Ɩ��t�����Ă��܂��B
�@�܂��C�����J���Ȃ͂���܂ōR����܂̏��F�́C�l�̂ւ̈��S���ƁC����̏k�����ʂ��K�{�����ł������̂ɑ��C���k�����Ă��������ʂɂȂ���Ȃ����Ƃ����邽�߁C�Q�O�O�U�N���牄�����ʂ̊m�F���`���Â��܂����B |
|
���Z�J���h�I�s�j�I���̏d�v��
�@���Ö@�͈�t�̊Ԃł��ӌ���������邱�Ƃ������C�悭������悤�ɁC�Z�J���h�I�s�j�I���i�厡��ȊO�̑��̈ӌ��j���ɂ��Ăق����ƍl���܂��B
�@�@
�@�A�����J�ł͈�t���Z�J���h�E�I�s�j�I���d���C�蒅���Ă��܂����C���{�ł͎厡��ɋC���˂����邱�Ƃ������C�܂����y���Ă��Ȃ��̂�����ł��B
�@
�@���Ö@������ɂ킽��C�������V�������Ö@�����X�ƊJ������Ă��邪�Âł́C���̎��W�ƃZ�J���h�E�I�s�j�I����������ɂȂ��Ă��܂��B
�@�ŋ߂ł̓Z�J���h�I�s�j�I�����̑�����݂���a�@�������Ă��܂��B���Ȃ��Ă��ς�p�����Ă��܂����ȂǁC���ƂŌ�����Ȃ����߂ɂ��C��l�̈�t�̈ӌ����ƍl�����C�ϋɓI�ɃZ�J���h�I�s�j�I�������߂܂��傤�B�@�@
|



